Ci sono delle volte in cui tutta una serie di coincidenze ti indicano che devi fare qualcosa… e tu non puoi esimerti da capire il messaggio e metterti al lavoro.
Negli ultimi mesi ci sono capitati nella pratica clinica diversi casi del genere e un carissimo amico, che non era minimamente informato di ciò ci ha indicato di fare attenzione ai meccanismi che andremo a descrivere nell’articolo, indicandoci tra l’altro delle risorse preziosissime per approfondire questi concetti che sono davvero poco conosciuti in ambito microbiologico e soprattutto sono sottovalutate le correlazioni tra queste infezioni speciali e gli esiti immunologici a lungo termine.
È necessario fare alcune importanti premesse:
- Dalla lettura dell’articolo non deve nascere una caccia a patologie inverosimili, soprattutto coinvolgendo i medici di famiglia richiedendo prescrizioni di esami rarissimi che non sono indicati
- L’articolo vuole essere una forma di chiarimento su meccanismi poco noti, va preso come una chiacchierata generica, non parla dei casi specifici, ma si tiene molto sui generis.
- L’articolo sarà per forza di cose un po’ tecnico, purtroppo tratta argomenti di microbiologia avanzata che per quanto possiamo cercare di spiegare in modo semplice, richiedono qualche competenza di batteriologia e di immunologia, ma di solito siamo bravissimi a trovare un linguaggio chiaro e comprensibile nonostante la difficoltà.
- La maggior parte degli studi a cui fa riferimento l’articolo sono molto recenti, 2018-2019, per cui si parla ancora di ricerca che non ha avuto tempo materiale di entrare in pratica clinica, ma che sta filtrando velocemente soprattutto tra reumatologi ed infettivologi.
Come ogni storia ci si aspetta che ci sia un protagonista, e qui ce n’è una fantastica, una delle massime conoscitrici di questi aspetti è una virologa immunologa americana che ci ha lasciato nel 2008, ma ha avuto una carriera accademica veramente di livello altissimo, che l’ha vista professoressa emerita nelle più importanti università americane, tra cui Harvard.
Tutta la sua attività di ricerca si è concentrata sulle “Stealth form”, cioè i batteri atipici che per il nostro sistema immunitario rappresentano delle sfide fuori dall’ordinario.
La scienziata in questione, una vetta altissima, è la Professoressa Lida Mattman, linkiamo qui la sua pagina wikipedia e la citazione al suo libro più famoso
https://en.wikipedia.org/wiki/Lida_Holmes_Mattman
https://academic.oup.com/cid/article-abstract/18/4/667/362635?redirectedFrom=fulltext
Cerchiamo di capire cosa intendiamo per “Stealth form” e per forme atipiche di batteri.
Noi siamo abituati a pensare ai batteri come entità microbiche che presentano una parete batterica ben precisa, siamo abituati a dividerli in gram+ o in gram- in base alla loro struttura che consente un diverso comportamento con la colorazione di Gram.
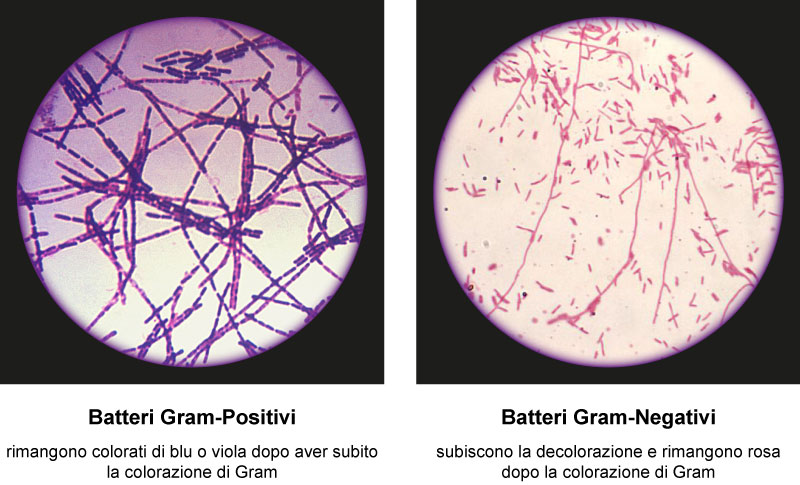
Esistono però batteri che hanno strutture assai diverse e quindi comportamenti replicazionali assai diversi, per fare un minimo elenco abbiamo:
I batteri endocellulari, che si replicano all’interno delle cellule, spesso e volentieri quelle immunitarie
- Chlamydie
- Rickettsie
- Ehrlichie
I batteri con caratteristiche di parete particolari
- Micobatteri, tra cui il più famoso è quello della tubercolosi, ma ne esistono molti altri
- Micoplasmi, che non hanno parete, ma una membrana molto ricca di steroli
- Ureaplasma
Batteri che possono sopravvivere senza parete, in una forma definita L-Form
- Stafilococchi
- Streptococchi
L’elenco potrebbe essere ancora molto lungo, ma intanto qui abbiamo raccolto i principali.
Per il nostro scopo è importante aggiungere qualche batterio più classico, ma che ha dimostrato essere comunque coinvolto in queste forme di artriti reattive:
- Shigelle
- Salmonelle
- Yersinie
- Campylobacter
Tutti questi batteri hanno la straordinaria capacità di eludere il nostro sistema immunitario che fa davvero molta fatica ad eliminarli, soprattutto i batteri endocellulari, e come spesso capita quando le infezioni diventano croniche e persistenti, nei soggetti predisposti, possono svilupparsi dei fenomeni autoimmuni che nascono da una parte dal tentativo di mettere in campo tutte le forze disponibili, e dall’altro delle strategie molecolari batteriche che possono nascondersi dentro cellule sane, ma lasciare il loro marchio antigenico sulle membrane self e creare meccanismi di mimetismo molecolare antigenico, o portare il sistema immunitario ad inserire un antigene self nella “banca dati” delle molecole da combattere, originando un danno autoimmune cronico che poi è difficilmente arrestabile.
Soprattutto nei soggetti HLA-B27+, che è già un HLA di rischio per le spondiloartriti e per le artriti psoriasiche, esiste un aumentato rischio anche di sviluppare una artrite reattiva come postumo di una infezione delle specie batteriche che abbiamo citato in precedenza, anche se per statistica la più comune artrite reattiva è proprio quella in seguito all’infezione da Chlamydia Trachomatis, e proprio su questo patogeno cercheremo di strutturare il discorso che in linea generale è estendibile agli altri, ma il meccanismo della clamidia è particolare e merita di essere citato nel dettaglio.
Chlamydia Trachomatis
La Clamidia è un batterio che si trasmette con rapporti sessuali non protetti, è spesso asintomatica o con minimi fastidi, e se dovessimo fare una ricerca sierologica a tappeto la gran parte della popolazione attiva sessualmente presenta gli anticorpi IgG ed IgM contro questo batterio.
La Clamidia è un batterio molto deficitario dal punto di vista metabolico, da sola non può produrre né ATP né molti aminoacidi, per cui ha necessità di penetrare nelle cellule eucariote e depredare le catene metaboliche cellulare per la sua sopravvivenza.
Nella sua forma ambientale la clamidia si fa piccola piccola, con un metabolismo quasi azzerato, la forma si chiama corpo elementare, mentre quando riesce ad infettare una cellula riattiva il suo metabolismo e forma il corpo reticolare.
Se tutto finisse qui sarebbe davvero facile, il problema è la sua capacità di eludere il sistema immunitario o la presenza dei normali antibiotici. Quando si sente minacciata prende un terzo tipo di forma che si chiama corpo aberrante che resiste molto bene agli antibiotici e ai meccanismi immunitari e sembra proprio che sia questa la forma più legata allo sviluppo di processi autoimmuni, tra cui le artriti, postumi all’infezione.
Lasciamo il link alla pagina MSD che descrive nel dettaglio le infezioni da clamidie
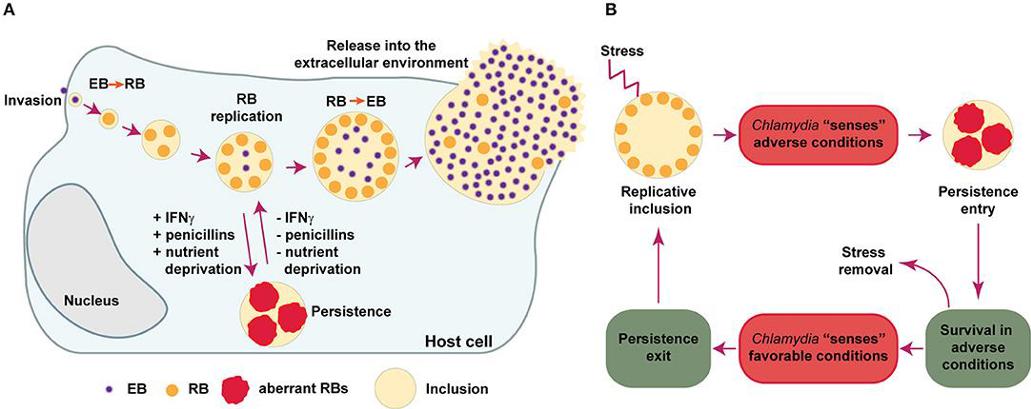
Questo è il ciclo replicativo, che è spiegato nel dettaglio in questo studio:
https://www.frontiersin.org/articles/10.3389/fmicb.2018.03101/full
Per i tecnici ne consiglio vivamente la lettura, è davvero una piccola perla.
A quanto pare la presenza di una infezione da clamidia, che credeteci non è facile da eradicare, comporta la produzione di una serie di citochine, tra cui forse la più importante da considerare è il TNF-alfa, che nei soggetti predisposti è un trigger importante nella genesi dell’artrite sieronegativa.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6783181/
Questo è uno studio che riguarda 1 solo paziente, che presentava una artrite reattiva che non rispondeva ai normali farmaci che si usano per il controllo dell’artrite, e aveva in contemporanea:
- HLA-B27
- IgM, IgA, IgG positive per la clamidia, ricordiamo che a livello diagnostico le più importanti solo le IgA che danno immunità mucosale, le altre sono poco indicative dello stato infettivo
La patologia artritica è andata in remissione con l’aggiunta di un farmaco biologico specifico per il TNF-alfa, e qui occorre un attimo di attenzione nell’interpretazione del risultato.
Lo studio ci dice che il TNF-alfa era la citochina che rappresentava la maggior capacità di innesco dell’artrite reattiva, se fosse stata una artrite normale non postuma ad infezione da clamidia, avrebbe risposto molto bene ai normai farmaci che si usano, nel caso dello studio in oggetto, colchicina e prednisone.
https://link.springer.com/article/10.1007%2Fs11926-019-0863-4
In questo recentissimo studio, pare che un trattamento antibiotico precoce, specifico per clamidia che ricordiamo richiede una terapia antibiotica particolare, sembra ridurre o annullare il rischio di sviluppare artrite reattiva, anche se sono necessari ulteriori studi.
Per trarre le conclusioni di questa lunga discussione possiamo dire che:
- Se l’artrite è comparsa qualche settimana dopo aver avuto rapporti a rischio
- Se migliora quando fate una terapia antibiotica per qualsiasi altro motivo
Potreste sospettare che si tratti di una artrite reattiva e che possa avere senso fare qualche analisi di approfondimento alla ricerca di una possibile infezione da clamidia.
Siccome sono evidenze scientifiche molto recenti, c’è una possibilità che chi vi segue non sia aggiornatissimo, per cui vi lasciamo la pagina MSD dedicata ai medici:
Visto che per noi questo sarà un anno molto ricco di aggiornamenti, parleremo sicuramente anche degli altri patogeni correlati alle artriti reattive, anche se per nostra esperienza, la maggior parte degli enterobatteri siano più connessi alle MICI.
Alleghiamo questo studio del 2018 che evidenzia come la presenza di klebsiella pneuomoniae nell’intestino sia correlata al morbo di Chron e alla RCU
https://onlinelibrary.wiley.com/doi/abs/10.1111/1751-2980.12595
Per concludere vorremmo fare due considerazioni:
- L’aspetto microbiologico correlato alle malattie autoimmuni è in questo momento sotto la lente di ingrandimento di moltissimi centri ricerca, questo ci fa ben sperare che molte correlazioni importanti verranno scoperte nei prossimo futuro con enormi nuove potenzialità terapeutiche molto mirate
- Non vorremmo che domani 40.000 persone corressero dal loro medico a cercare la clamidia, lo scopo del post era descrivere un fenomeno poco conosciuto, non generare paure collettive
- dulcis in fundo, proteggete i rapporti
Con questo ultimo articolo si chiude il 2019, state in attesa per un grandissimo 2020